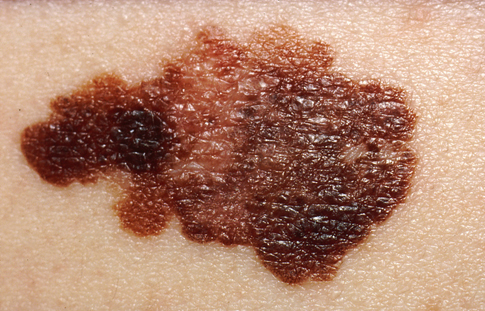
Την έγκριση της ΕΕ έλαβε νέα θεραπεία για το μεταστατικό μελάνωμα
Η Ευρωπαϊκή Επιτροπή χορήγησε άδεια κυκλοφορίας στην δραστική ουσία dabrafenib ως μία από του στόματος στοχευμένη θεραπεία που ενδείκνυται ως μονοθεραπεία του ανεγχείρητου μελανώματος ή του μεταστατικού μελανώματος σε ενήλικες ασθενείς με μετάλλαξη BRAF V600.
Spotlight
-

Η Μέγκαν Φοξ φωτογραφήθηκε χωρίς μακιγιάζ και τρόμαξαν να την αναγνωρίσουν
-

«Τεράστια ανησυχία» ΠΟΥ για κίνδυνο εξάπλωσης της γρίπης των πτηνών στους ανθρώπους
-

Δημοσκόπηση: Παραμένουν οι «κόκκινες κάρτες» για την κυβέρνηση – Ισχυρή η δυναμική του «Κανένα»
-

Αυτό που θα δεις πρώτα στην εικόνα αποκαλύπτει πολλά για την προσωπικότητά σου
Η dabrafenib δεν ενδείκνυται για τη θεραπεία ασθενών με BRAF φυσικού τύπου μελάνωμα. Πριν τη χορήγηση της dabrafenib, πρέπει να επιβεβαιωθεί η μετάλλαξη BRAF V600 στους ασθενείς, κατόπιν έγκυρης εξέτασης.
Η dabrafenib είναι ένας αναστολέας κινάσης που στοχεύει το BRAF, βασικό συστατικό ενός βιολογικού μονοπατιού στον οργανισμό που ρυθμίζει τη φυσιολογική ανάπτυξη και τον θάνατο των κυττάρων, συμπεριλαμβανομένων των δερματικών κυττάρων. Με τη βοήθεια μιας διαγνωστικής εξέτασης μπορούν να εντοπιστούν οι ασθενείς με ανεγχείρητο ή μεταστατικό μελάνωμα που έχουν τη μετάλλαξη BRAF V600, γεγονός που τους καθιστά κατάλληλους για αυτή τη θεραπεία.
Σύμφωνα με τον Παγκόσμιο Οργανισμό Υγείας, 200.000 άνθρωποι παγκοσμίως διαγνώστηκαν με μελάνωμα το 2008, νούμερο που υπολογίζεται να αυξηθεί σε 233.000 έως το 2015. Η διάμεση επιβίωση καθώς και το ποσοστό επιβίωσης στο ένα έτος για τους ασθενείς με μεταστατικό μελάνωμα, οι οποίοι λαμβάνουν χημειοθεραπεία, είναι 12 μήνες και 49% αντιστοίχως.
Η άδεια κυκλοφορίας της dabrafenib βασίζεται σε αποτελέσματα από αρκετές πολυκεντρικές παγκόσμιες δοκιμές. Μία από αυτές τις δοκιμές ήταν μια μελέτη Φάσης III, η BREAK-3, στην οποία η θεραπεία με dabrafenib συγκρίθηκε με την dacarbazine (χημειοθεραπεία) σε 250 ασθενείς, που δεν είχαν λάβει προηγούμενη θεραπεία, θετικούς στη μετάλλαξη BRAF V600E, με ανεγχείρητο ή μεταστατικό μελάνωμα. Στην προγραμματισμένη ανάλυση της BREAK-3, τον Δεκέμβριο του 2011, η dabrafenib μείωσε τον σχετικό κίνδυνο εξέλιξης της νόσου ή του θανάτου κατά 70% σε σύγκριση με την dacarbazine (95%, CI: 0,18, 0,51, p<0,0001). Τα δεδομένα της μελέτης έδειξαν ένα διάμεσο διάστημα επιβίωσης χωρίς εξέλιξη της νόσου της τάξης των 5,1 μηνών με dabrafenib (95%, CI: 4,9, 6,9) σε σύγκριση με 2,7 μήνες για την dacarbazine (95%, CI: 1,5, 3.,2) (δεδομένα αποκοπής του 2011).
Σε μία μεταγενέστερη ανάλυση από τον Ιούνιο του 2012, η dabrafenib μείωσε τον σχετικό κίνδυνο εξέλιξης της νόσου ή του θανάτου κατά 63% σε σύγκριση με την dacarbazine (95%, CI: 0,24, 0,58, P<0,0001). Τα δεδομένα έδειξαν διάμεσο διάστημα επιβίωσης χωρίς εξέλιξη της νόσου της τάξης των 6,9 μηνών (95%, CI: 5,2, 9,0) σε σύγκριση με 2,7 μήνες για την dacarbazine (95%, CI: 1,5, 3,2). Μια περαιτέρω μεταγενέστερη ανάλυση, από τον Δεκέμβριο του 2012, έδειξε ότι η συνολική επιβίωση στους 12 μήνες ήταν 70% με την dabrafenib, έναντι του 63% με την dacarbazine (HR = 0,76, 95%, CI: 0,48, 1,21).
Οι ασθενείς με μελάνωμα με μεταλλάξεις διαφορετικές από τη μετάλλαξη V600E αποκλείστηκαν από τη δοκιμή BREAK-3 και όσον αφορά στους ασθενείς με μετάλλαξη V600K που συμμετείχαν σε μελέτες μονού σκέλους, η δραστηριότητα εμφανίζεται χαμηλότερη από ό,τι στους όγκους V600E.1
Στην Ευρωπαϊκή Ένωση (ΕΕ), η dabrafenib εγκρίνεται πλέον ως μονοθεραπεία κατά τη θεραπεία ενήλικων ασθενών με ανεγχείρητο ή μεταστατικό μελάνωμα με μετάλλαξη BRAF V600, εφόσον έχει ανιχνευτεί με έγκυρη εξέταση. Η dabrafenib έχει λάβει ανάλογη έγκριση στις ΗΠΑ, τον Καναδά και την Αυστραλία.
Το προφίλ ασφαλείας της dabrafenib βασίζεται σε δεδομένα από πέντε κλινικές μελέτες μονοθεραπείας και περιλαμβάνει 578 ασθενείς με μελάνωμα. Η πιο συχνές ανεπιθύμητες ενέργειες (ADRs) (≥ 15%) που αναφέρθηκαν με το dabrafenib ήταν η υπερκεράτωση (μια πάθηση που προκαλεί καλοήθη πάχυνση του δέρματος ή δερματικές βλάβες), η κεφαλαλγία, η πυρεξία (πυρετός), η αρθραλγία (πόνος στις αρθρώσεις), η κόπωση, η ναυτία, το θήλωμα του δέρματος (μια πάθηση που προκαλεί καλοήθη ανάπτυξη του δέρματος), η αλωπεκία (απώλεια μαλλιών), ο κνησμός και ο έμετος.
health.in.gr
Ακολουθήστε το in.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις





























 Αριθμός Πιστοποίησης Μ.Η.Τ.232442
Αριθμός Πιστοποίησης Μ.Η.Τ.232442